Accueil > 9999 TS > TS : Chapitre 3 Réactions par échange de protons
TS : Chapitre 3 Réactions par échange de protons
vendredi 21 septembre 2018, par
L’ion H+ n’existe pas en solution, il est immédiatement capté par une des innombrables molécules d’eau.

- Capture
L’échelle de pH est une échelle logarithmique.

- Capture02
Exemple de réaction d’un acide avec l’eau :

- reaction1
Exemple de réaction d’une base avec l’eau :

- reaction2
Comptes-Rendus de TP :
Jeudi 6 octobre : TP n°5 détermination de la constante d’acidité d’un acide faible
Résultats obtenus pour une solution d’acide éthanoïque de concentration 1,0.10-2 mol/L. l’abscisse x vaut log([ion éthanoate]/[acide éthanoïque])
Valeur du pKA = 4,46 +- 0.07
Les pH-mètres du lycée ont tendance à mesurer 0,2_0,3 unités de pH trop bas.
Série de compte-rendus réalisés les années précédentes :
Document général techniques de TP et protocoles :
TP n°6 jeudi 14 octobre
![]() construction expérimentale des courbes de prédominance des formes acides et basiques d’un indicateur coloré.
construction expérimentale des courbes de prédominance des formes acides et basiques d’un indicateur coloré.
![]() détermination de son pKa
détermination de son pKa
![]() méthode spectrophotométrique
méthode spectrophotométrique
TP n°4 jeudi 1 octobre
![]() premières mesures de pH
premières mesures de pH
![]() distinction acide fort/acide faible
distinction acide fort/acide faible
![]() effet de la dilution sur le pH
effet de la dilution sur le pH
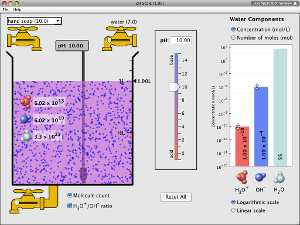
Une animation pour faire le lien entre la valeur du pH mesuré et la présence des espèces chimiques, H3O+, OH- et H20.
![]() en haut à gauche, choisir un milieu
en haut à gauche, choisir un milieu
![]() règle centrale valeur du pH
règle centrale valeur du pH
![]() à droite on peut fixer les concentrations ( à noter que [H3O+]x[OH-] est effectivement constant)
à droite on peut fixer les concentrations ( à noter que [H3O+]x[OH-] est effectivement constant)
![]() en bas à gauche cocher visualisation des molécules
en bas à gauche cocher visualisation des molécules
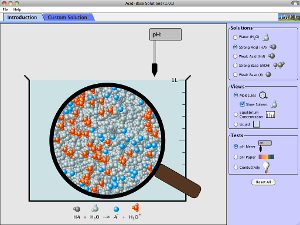
Une autre pour visualiser la différence entre acide faible/fort et base forte/faible via les états d’équilibres de la réaction avec l’eau